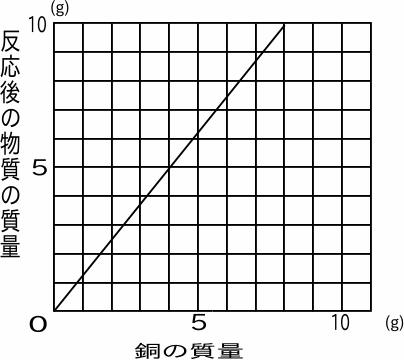
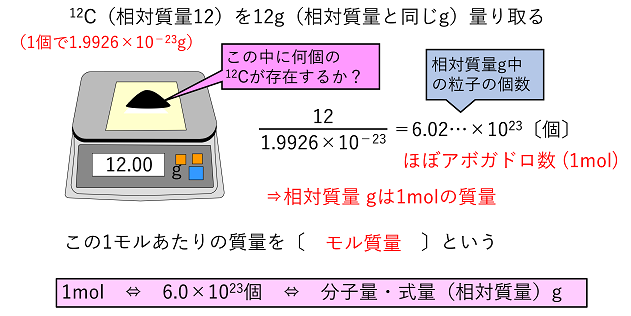
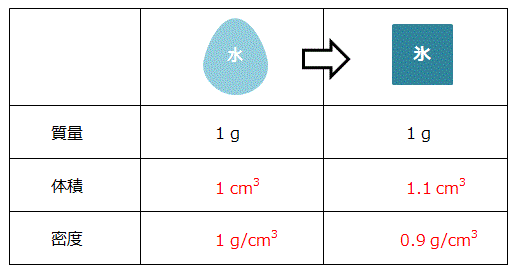
6/5/17 モル質量 とは、ある分子や原子を1 mol集めたときの質量です。 1 molあたりの質量になるので、 単位は質量をmol(物質量)で割った、「g / mol」になります。 自然に存在する原子を1 mol集めたときの質量(原子量)の多くは数g~数100gになるため、23/5/21 3つの公式の覚え方 質量=体積×密度 密度=質量÷体積 体積=質量÷密度 という3つの公式は、まとめて1つの図で表すことができます。 比重の 軽い ものの方が 重さが軽く、 比重の 重い ものの方が 重さが重くなります。13/2/ 未反応の銅の質量の求め方! 質量の増加分から化合した酸素の質量を求める。 040g-045g=005g 化合した酸素の質量から反応した銅の質量を求める。 4:1=x:005 x=0g 銅全体の質量から反応した銅の質量を引いて未反応の銅の質量を求める。

物質量molの超解説 理系ラボ
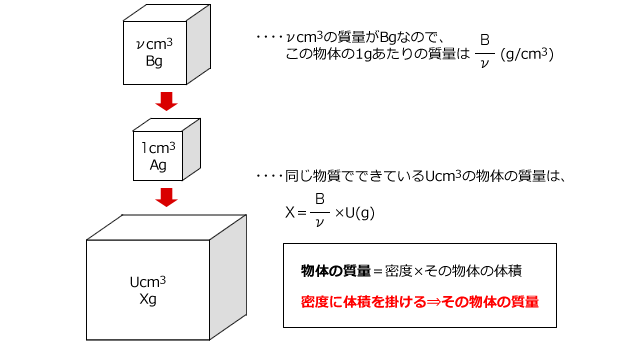
物質の質量の求め方
物質の質量の求め方-例えば、CO 2 のモル質量は約44 g/mol です(炭素のモル質量は12 g/molで、酸素のモル質量は16 g/molなので、合計は12 16 16 = 44となります)。 04mol CO 2 x 44 g/mol CO 2 = 367g。5/7/21 原則として、それらはF x NO y * 5 H 2 Oの形の複雑な化学構造である。 この場合の溶質の質量分率の求め方は異なります。 第一に、結晶性水和物が関与するいかなる作業においても、結晶性水和物自体の質量m crおよび無水物質の質量F x NO yが示される。



1
質量パーセント濃度 をどのように求めるかというと、次の式に当てはめます。 質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×100物質1molあたりの質量は、原子量・分子量・式量に単位〔g〕をつけたもの まずは、 (1)です。 問題文より、アルミニウム Al の原子量は27です。 ということは、アルミニウム1molあたりの質量は、 27g です。 このことから、比例式を立ててみましょう。 1mol27g= 3mol x g x=81 よって、答えは、 81g です。 次は、 (2)です。3原子核の質量 質量公式, フェルミガス模型 4核物質の状態方程式 対称核物質の状態方程式, 対称エネルギー, 対称エネルギーの実験的制限 5クォーク物質とハドロン物質 クォーク物質ハドロン物質 6中性子星と核物質状態方程式
質量を正確に導くことができる。この原子の質量を それぞれ「物質量分率」および「物質量濃度」)などの計 算方法を学生時代に学習された方も多いと思う。近年、 環境分析などで、種々の物質の濃度の正確な測定が求め られている。28/8/18 質量数12の炭素の中性子数は、 126=6です 。覚えなくていいですが、 中性子数=質量数ー原子番号 で求められます。 質量数と原子番号を元素記号で表すと? このように、左上が質量数、左したが原子番号を表します。1/6/ 性物質の量を示す目安 として使われてる。それなら、どうして「kg」や「g」 といった 質量 (いわゆる重さ) の単位を使わない のだろうか。 おそらくそれは、質量よりも 放射能で表 す方が実用的 だからだろう。何 g ある
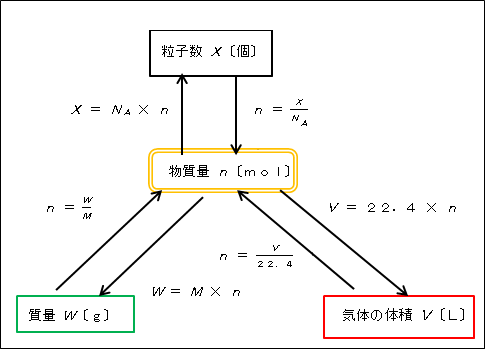
例えば,モル質量が g/mol と求められれば,この気体の分子量は になります.この値は最 も軽い気体の水素の分子量と一致しますから,このガスボンベには水素が詰まっていると判断できま す7/2/17 (質量パーセント濃度 % )= (溶質の質量)÷(溶液の質量)×100× mol = g より,モル質量〔g/mol〕に物質量〔mol〕を掛けることで,質量〔g〕を求めることができます( w = n × M )。 g ÷ = mol より,質量〔g〕をモル質量〔g/mol〕で割ることによって,物質量〔mol〕を求めることができます( n = )。




質量パーセント濃度の求め方とモル濃度の違い



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム
はじめに ここでは、溶液の濃度を表す単位である質量パーセント濃度、モル濃度そして質量モル濃度の単位、求め方についてまとめています。 質量パーセント濃度 小学校や中学校で、食塩水の濃度を求めてみましょうという問題を解いたのを記憶しれいる人も多いかと312 質量の表し方 Z 個の電子を伴った中性原子の質量を,原子核の質量数A と原子番号(陽子数)Z を用い てM(A,Z)で表すことにする.この表し方を用いると,中性子の質量はm n =M(1,0),水 素原子の質量はm H =M(1,1),原子質量単位の基準となる中性炭素原子の7/2/17 密度の出し方は次の公式で計算できちゃうよ。 密度 = 質量 ÷ 体積




1分でわかる質量パーセント濃度の公式や求め方 基本を登録者数95万人人気講師がわかりやすく解説 ページ 4 4 Study Z ドラゴン桜と学ぶwebマガジン




高校生物基礎 腎臓のイヌリン濃縮率や原尿量などの計算問題の解き方 高校生物の学び舎
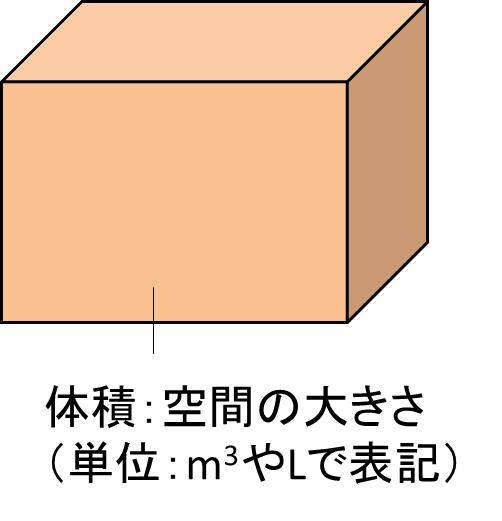
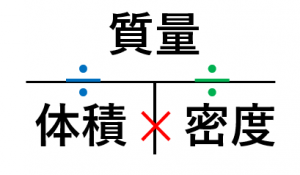
「質量 ÷ 体積」 で計算していますよね。 これが「密度の求め方」なんです。 物質の質量(g) 密度(g/cm³)= 物質の体積(cm³) 「g/cm³」は 「グラム毎 立方センチメートル」 と読みます。 1mol (今ある水素の物質量):x mol(必要な酸素の物質量) = 2mol(水素の物質量) :1mol(酸素の物質量) 2x = 1 →x = 1÷2 = 05 mol物質移動係数の求め方(1) • 伝熱実験(表面温度、気流温度、熱流束の測定) • 決定した伝熱係数(温度境界層厚み)を レイノルズ数Reとプラントル数Prの関数として整理 • Prをシュミット数Scに置き換える 熱移動と物質移動のアナロジーを活用




中学理科 還元されずに残った酸化銅の質量 の求め方 なるほどの素




2 の未反応の銅粉末の質量の求め方を教えて頂きたいです 答えは0 52gです Clear
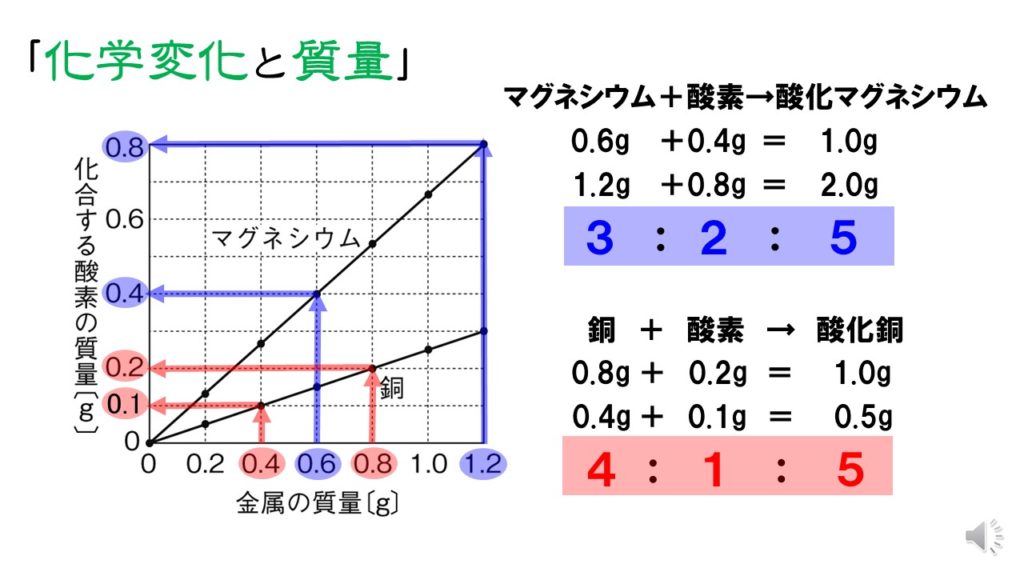
物質の量は質量(g)よりも物質量(mol)が化学計算には使われます。 物質量(mol)と原子分子の粒子の数の計算問題 を参考にして、 物質の粒子の数や質量から物質量に換算する練習はしておいた方規制物質の最大許容濃度はANNEXⅡ(付属書Ⅱ)で物質ごとに決められています。 タイトルには「weight in homogeneous materials」とあり、直訳すると「均質材料(均一材料)中の重さ」となり、均質材料中の重さによって濃度が決められていることが分かります。化学反応の前後において,物質の質量の総和は変わらない。 例:1( g )の水素と8( g )の酸素で9( g )の水ができる。 水素 + 酸素 → 水 定比例の法則 (1799年 プルースト) 化合物を構成する成分元素の質量比は常に一定である。




これでできる モル Mol 計算 化学基礎 最大の難所を突破しよう 化学 アイドル好きのホームページ



1
24/3/06 Re構成物質(成分)含有量の計算方法を教えて下さい isisan ( >CAD内のコマンドで体積・表面積を求め、JISハンドブック >を参照し、比重を掛けて質量を求める・・・ ・・・そういう方式では比重は使用しますが・・「報告」に




溶液の性質 水和水をもつ固体の溶解度の求め方を教えてください 化学 定期テスト対策サイト
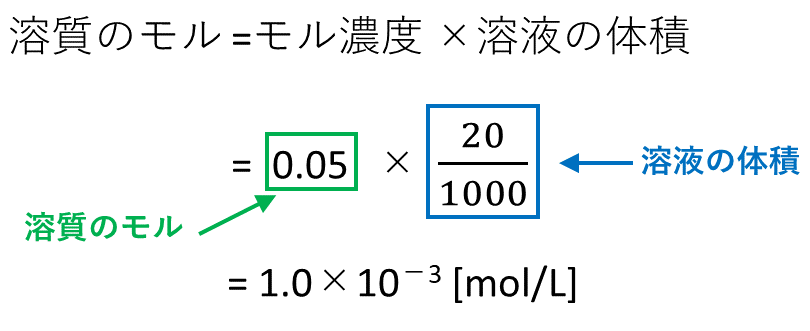



5分でわかる モル濃度と密度 質量パーセント濃度の考え方を図と練習問題付きで徹底解説 サイエンスストック 高校化学をアニメーションで理解する




物質 気体 水溶液 密度はどのように求めるのか 中学理科 定期テスト対策サイト




Bar3 H10 C12 N14 016 Descubre Como Resolverlo En Qanda




中2化学 マグネシウムの燃焼 計算問題 Hiromaru Note




物質量 Mol とモル質量と原子量の関係




密度 体積 質量の換算式と求め方 計算問題 モッカイ




中学理科 還元されずに残った酸化銅の質量 の求め方 なるほどの素




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




最新物質 の 質量 の 求め 方 最高のぬりえ
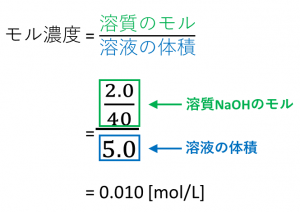



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine



溶質を求める
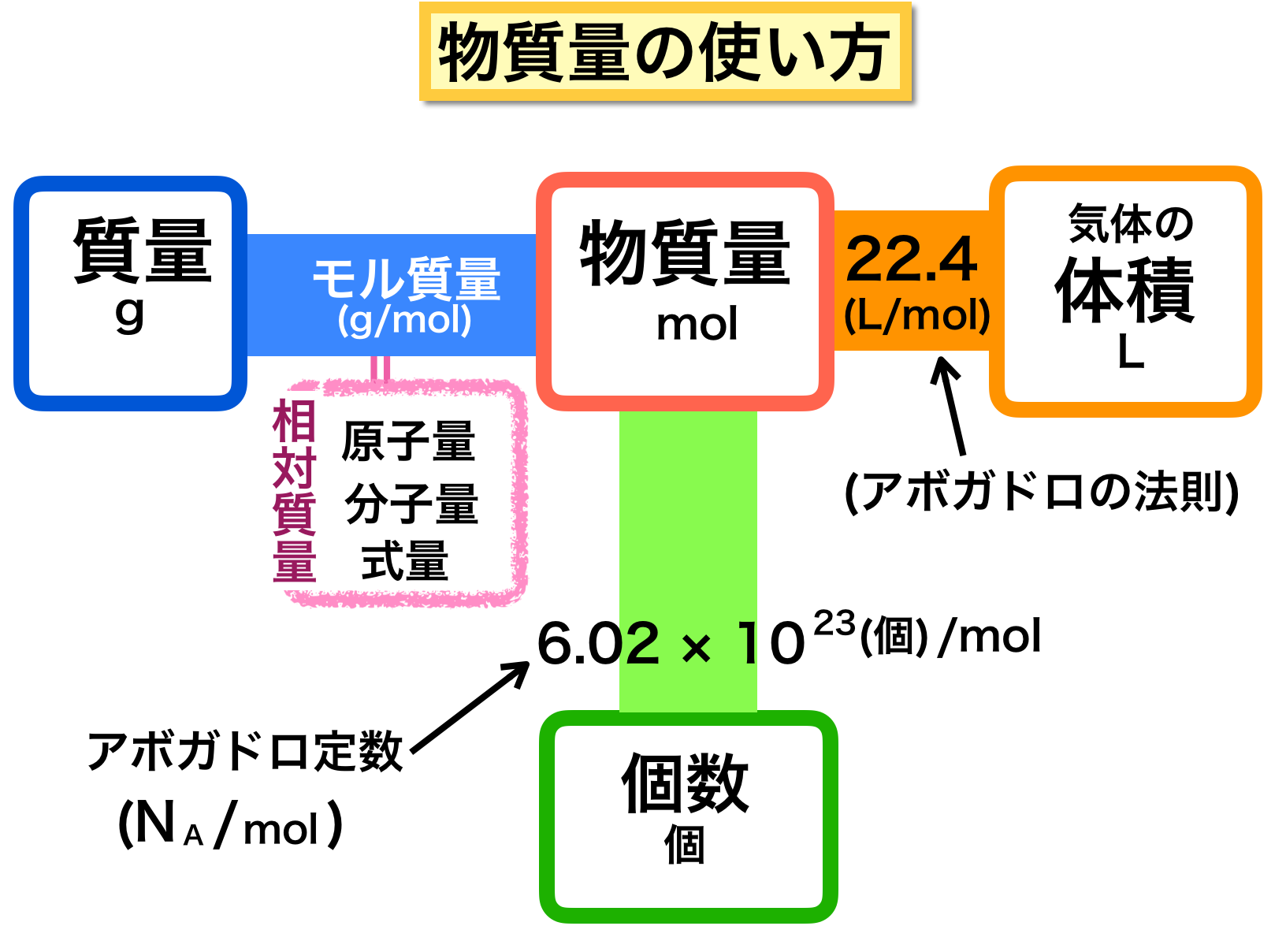



大気の平均分子量と物質量 Mol のまとめ 色と形で気象予報士




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



1



アボガドロ数の測定法



密度と体積の関係は 1分でわかる意味 違い 計算と覚え方 質量との関係



物質量 の指導における イメージ化 化学授業実践記録 アーカイブ一覧 理科 高等学校 知が啓く 教科書の啓林館




4 6 溶液の濃度 おのれー Note




中学理科 3分でわかる 密度の求め方 出し方の計算公式 Qikeru 学びを楽しくわかりやすく



1




中1理科 密度の計算 3パターンの計算方法 Pikuu



放射能と吸収線量の測定単位




中学理科 水溶液の濃度と飽和 溶解度 偏差値40プログラマー




高校化学基礎 モル質量とは 映像授業のtry It トライイット




水の質量と体積を変換 換算 する方法 計算問題を解いてみよう 水の重さの求め方




化学 質量数と相対質量 オンライン無料塾 ターンナップ



化学変化と質量



密度 体積 質量の換算式と求め方 計算問題 モッカイ




中学理科 3分でわかる 密度の求め方 出し方の計算公式 Qikeru 学びを楽しくわかりやすく




モル比熱 高校物理をあきらめる前に 高校物理をあきらめる前に




高校化学 質量と物質量 相対質量の求め方 オンライン無料塾 ターンナップ Youtube




原子量とは 求め方や単位も見やすい図と例で即理解 分子量との違いも 高校生向け受験応援メディア 受験のミカタ



物質量
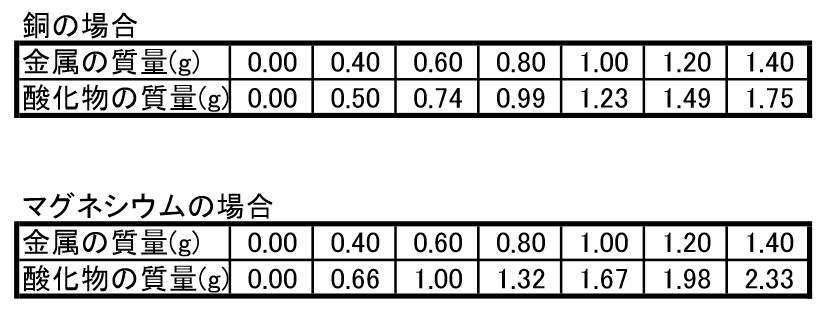



化学変化と物質の質量4 質量変化の規則性 後編 理科とか苦手で




質量パーセント濃度の計算問題集 基本編 Menon Network
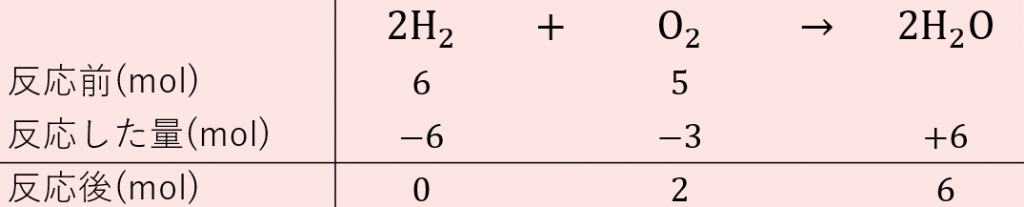



物質量molの超解説 理系ラボ
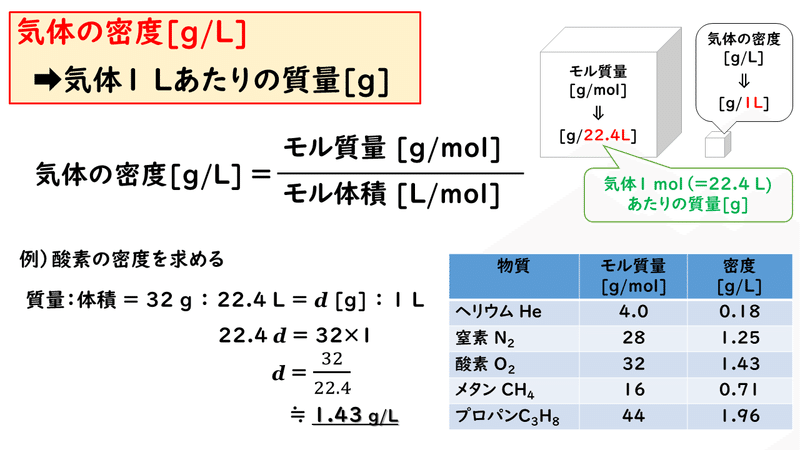



4 5 気体の密度と平均分子量 おのれー Note
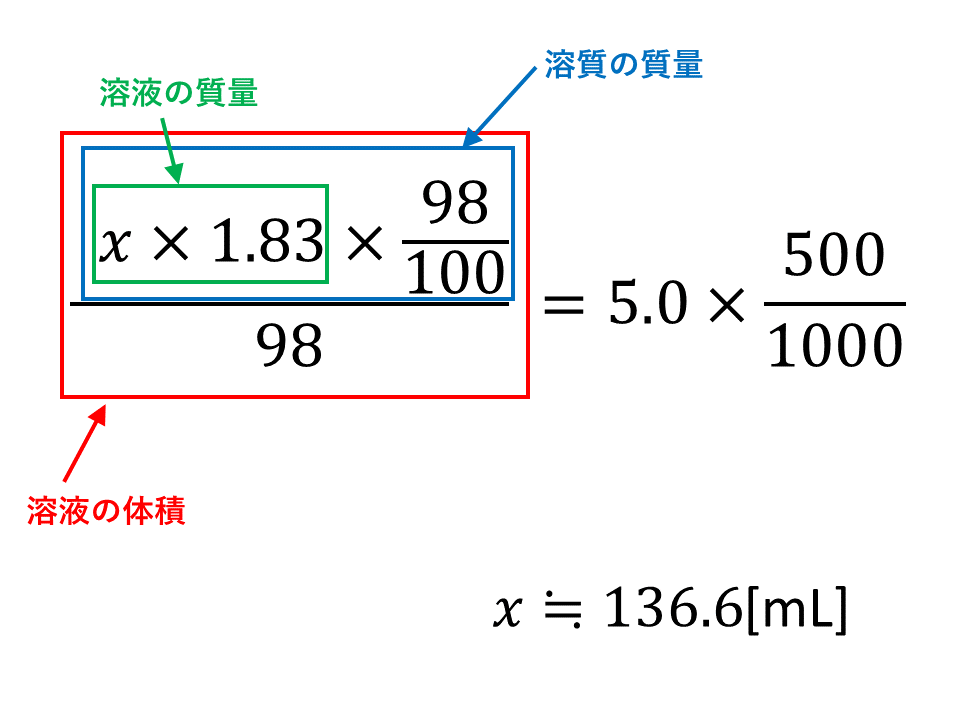



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine
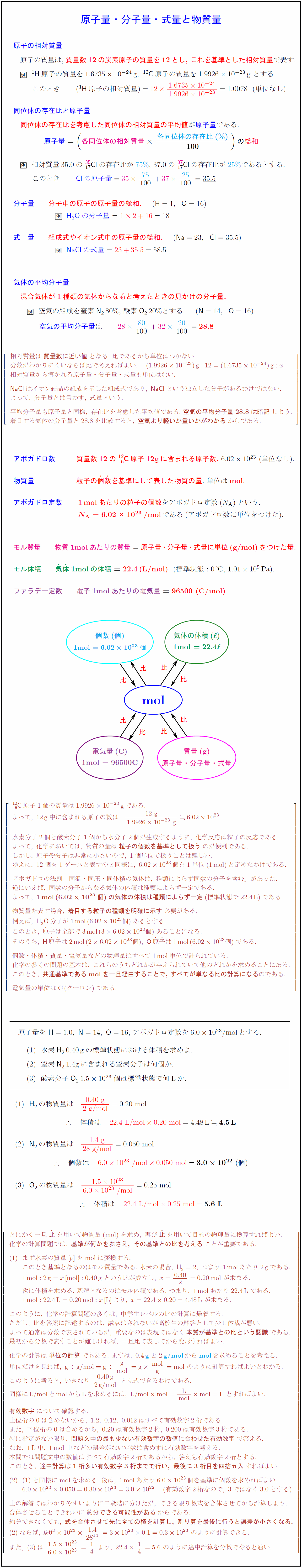



高校理論化学 原子量 分子量 式量と物質量 Mol 化学計算の基本 受験の月



物質量の計算の公式を 木の下ハゲじじいの きはじ 風にやると Yahoo 知恵袋



相対質量 原子量 分子量 式量 理解できてる 受験メモ




中2 理科 中2 13 化合する物質の割合 計算編 Youtube




理科 中1 19 密度の計算 Youtube




分子1個の質量の求め方は なぜこのようになるのでしょうか 初歩的な質問ですみません Clear
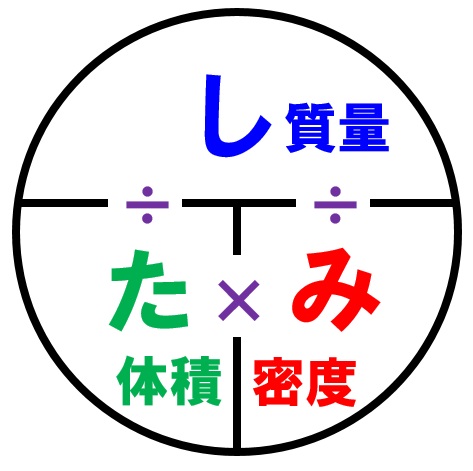



中1理科 密度の求め方3パターンの計算方法 Examee



質量の求め方は 1分でわかる公式と求め方 体積 密度との関係 求め方
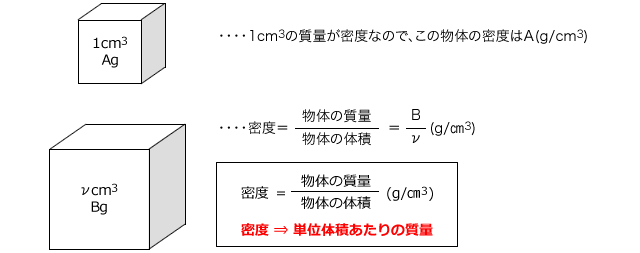



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム
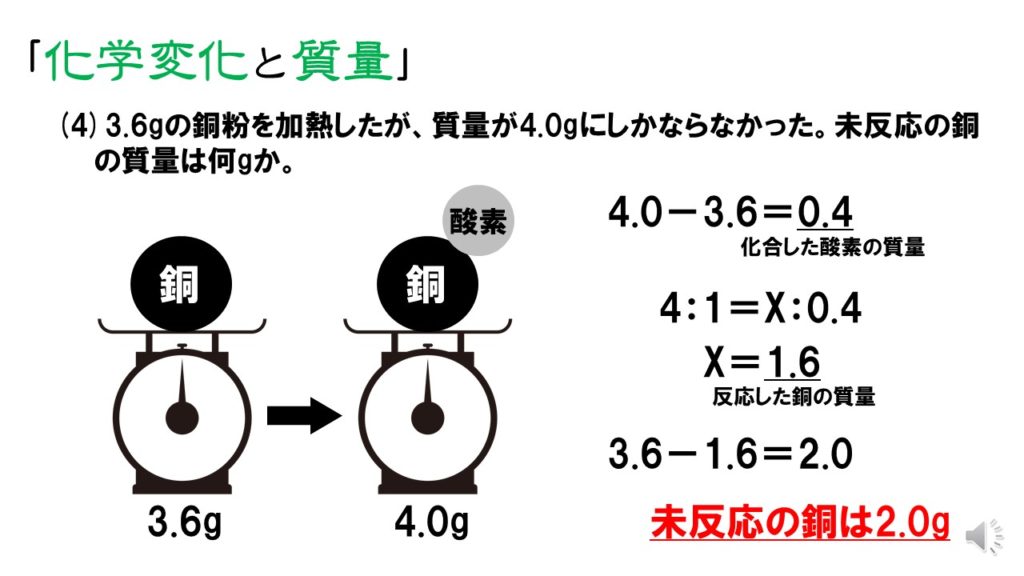



中2理科 化学変化と質量 銅とマグネシウムの計算 Pikuu



中2理科 化学変化と質量の計算問題 Examee




化学 原子量の計算方法 オンライン無料塾 ターンナップ



中2理科 化学変化と質量の計算問題 Examee




4 6 溶液の濃度 おのれー Note




高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月




原子量 分子量 式量の違いと モル質量の計算での求め方 使い方をわかりやすく解説



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Relative Mass




物質量とモル質量の違いは 計算問題を解いてみよう 演習問題




窒素1molは何グラムで体積はいくら 窒素のリットルとグラムの変換方法は 窒素1モルの体積や重さ 質量 やモル質量の計算方法 ウルトラフリーダム




質量や原子数分子数と物質量 Mol を変換する計算問題




化学基礎 物質の変化07 モル質量の求め方 13分 Youtube



1
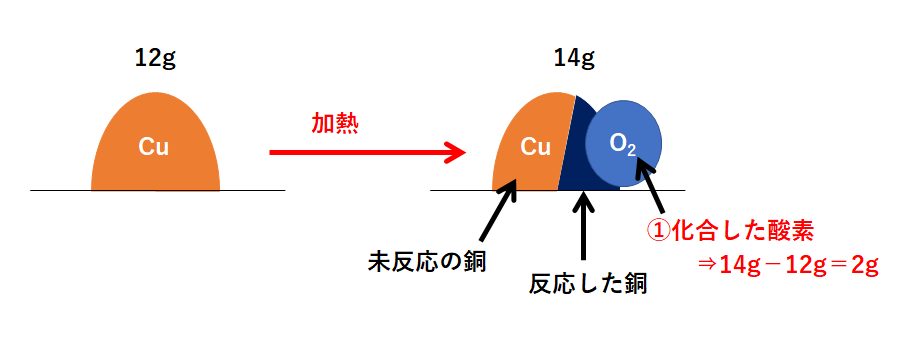



中2化学 定比例の法則 未反応 混合物 中学理科 ポイントまとめと整理




問題 マグネシウム原子1個の質量を求めよ Clear
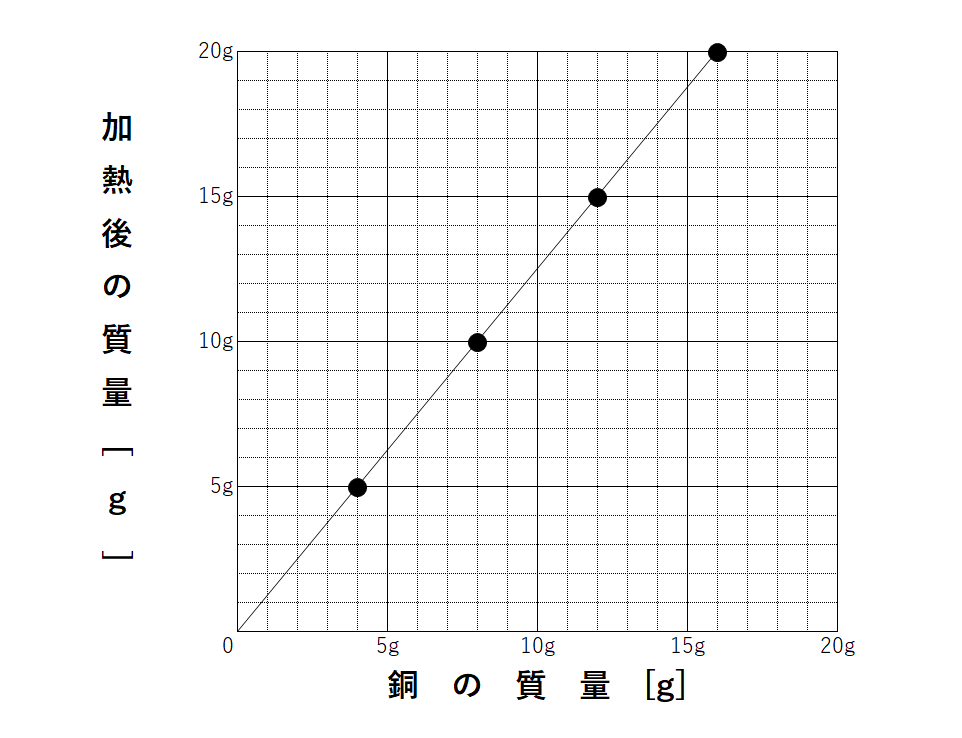



中2化学 定比例の法則 酸化 中学理科 ポイントまとめと整理




高校化学基礎 モル質量の計算 練習編 映像授業のtry It トライイット




高校化学 質量モル濃度 映像授業のtry It トライイット




化学変化と質量 無料で使える中学学習プリント
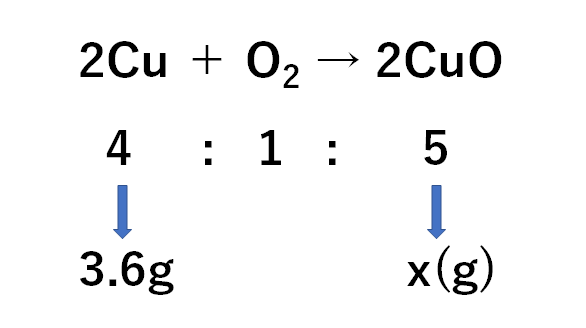



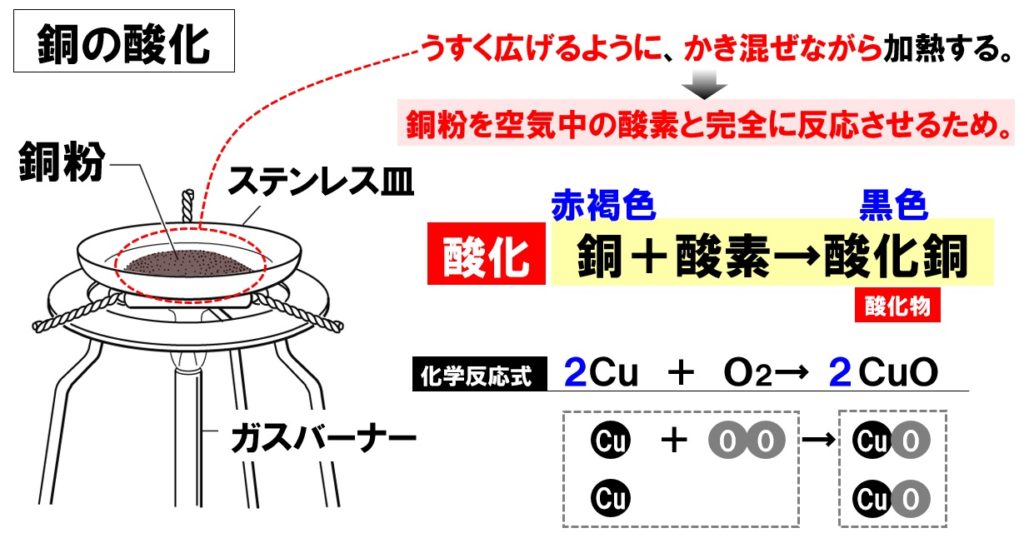
中2化学 定比例の法則 酸化 中学理科 ポイントまとめと整理




密度の公式 求め方 しみた の法則 無料プリント 中学理科 Yattoke プリント カード



質量 密度 体積それぞれの求め方 具体例で学ぶ数学



物質量の計算の公式を 木の下ハゲじじいの きはじ 風にやると Yahoo 知恵袋




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ




高校化学 相対質量 写真のように12cを12として 1hの相対質量を求め Okwave




濃度のはなし 高校生向け モル濃度と質量モル濃度について 学習内容解説ブログ



密度と比重量と比重の違い




Lihat Cara Penyelesaian Di Qanda




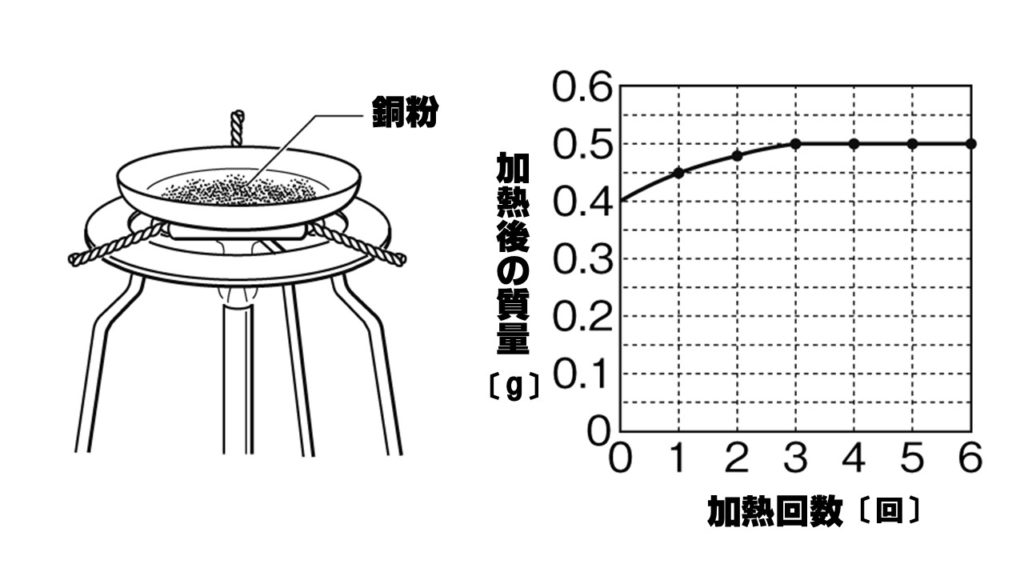
中2化学 銅の酸化 計算問題 Sciencenote Jp




最新物質 の 質量 の 求め 方 最高のぬりえ




密度の公式 覚え方は し み た でバッチリ 中学数学 理科の学習まとめサイト




いろいろな物質と密度 無料で使える中学学習プリント



質量と比重




密度の公式 物質の密度の求め方は しみた の法則 中学理科 Yattoke 小 中学生の学習サイト




質量保存の法則の計算問題 加熱が不十分だったとき 塾の質問箱




中2理科 銅とマグネシウムの酸化と質量 計算問題 2学期中間テスト用 赤城 ᐡᐤᐡ




物質量の求め方とは 単位や計算問題も解説 高校生向け受験応援メディア 受験のミカタ




最新物質 の 質量 の 求め 方 最高のぬりえ




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




物質量molの超解説 理系ラボ




物質量とモル質量の違いや アボガドロ定数をわかりやすく解説




高校化学基礎 相対質量の計算 映像授業のtry It トライイット



中2理科 化学変化と質量 銅とマグネシウムの計算 Pikuu




エ で酸化せずに残ったマグネシウムの質量の求め方を教えてください Clear




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく
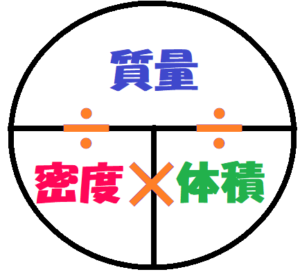



中学校理科の公式一覧
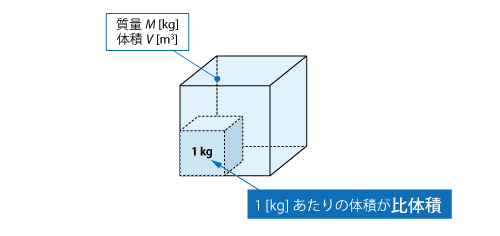



比体積




化学基礎 基本の物質量 Mol 計算について Study By Tmt


